Class 10 Science Lesson 5 I মৌলৰ পৰ্যাবৃত্ত শ্রেণীবিভাজন I [Periodic Classification of Element]
প্রশ্ন 1. নিউলেণ্ডছৰ অষ্টকৰ স্তম্ভবোৰত ড’বাৰেইনাৰৰ ট্ৰায়াড আছিলনে? তুলনা কৰা আৰু বাছি উলিওৱা।
উত্তৰ: আছিল। সেইটো হ’ল— [Li, Na, K]
প্রশ্ন 2. ড’বাৰেইনাৰৰ শ্ৰেণীবিভাজনৰ সীমাৱদ্ধতাবোৰ কি কি আছিল?
উত্তৰ : ড’বাৰেইনাৰে সেই সময়লৈকে জ্ঞাত আটাইবোৰ মৌলকেই ট্রায়াড হিচাপে শ্রেণীভুক্ত কৰিব পৰা নাছিল। তেওঁৰ সময়লৈকে জনা যোৱা মৌলসমূহৰ মাজৰ পৰা তেওঁ মাত্র তিনিটা ট্রায়াডহে চিনাক্ত কৰিছিল। সেয়েহে ট্রায়াড় হিচাপে শ্রেণীবিভাজনৰ এই পদ্ধতিটো ব্যৱহাৰোপযোগী নাছিল।
প্রশ্ন 3. নিউলেগুছৰ অষ্টক সূত্ৰৰ সীমাবদ্ধতাবোৰ কি কি আছিল? [HSLC 2020,2022]
উত্তৰ : (i) অষ্টক সূত্ৰটো কেৱল কেলছিয়াম পর্যন্তহে প্রজোয্য হোৱা দেখা গৈছিল। কেলছিয়ামৰ পাছত অষ্টম মৌল একোটাৰ ধৰ্মবোৰ প্ৰথমটোৰ সৈতে একে নাছিল।
(ii) নিউলেণ্ডছে প্ৰকৃতিত কেৱল 56 টা মৌল থকা বুলিহে জানিছিল আৰু ভৱিষ্যতেও আৰু অধিক মৌল আৱিষ্কাৰ নহ’ব বুলিয়েই ধৰিছিল। কিন্তু পৰৱৰ্তী কালত অনেক নতুন মৌল আৱিষ্কাৰ হোৱাত এইবোৰৰ ধৰ্মবোৰ অষ্টক সূত্ৰৰ লগত খাপ খোৱা নাছিল।
(iii) নিউলেণ্ডছে তেওঁৰ তালিকাখনত মৌলবোৰ সজাওঁতে কেৱল একেটা স্থানতে দুটাকৈ মৌলক স্থান দিয়াই নহয়, ধৰ্মৰ মিল নথকা কিছুমান মৌলকো একেটা স্তম্ভতে অন্তৰ্ভুক্তও কৰিছিল।
প্রশ্ন 4. মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকাখন ব্যৱহাৰ কৰি তলত দিয়া মৌলকেইটাৰ অক্সাইডৰ সংকেত নিৰ্ণয় কৰা। [HSLC 2018]
K, C, Al, Si, Ba
উত্তৰঃ K2O, CO2, Al2O3, SiO2, BaO
প্রশ্ন 5. গেলিয়ামৰ উপৰিও আন কোনকেইটা মৌলৰ বাবে মৌলকেইটা আৱিষ্কৃত হোৱাৰ পূৰ্বেই মেণ্ডেলিভে তেওঁৰ তালিকাত ঠাই ৰাখি থৈ গৈছিল? (যিকোনো দুটা) [HSLC 2018, 2022]
উত্তৰ : স্কেন্ডিয়াম, জার্মেনিয়াম।
প্রশ্ন 6. মেণ্ডেলিভে তেওঁৰ পৰ্যাবৃত্ত তালিকাখন যুগুতাওঁতে মানি চলা নীতিবোৰ কি কি আছিল?
উত্তৰ: (i) তেওঁ মৌলসমূহক সিহঁতৰ পাৰমাণৱিক ভৰৰ বৰ্ধিত ক্ৰমত সজাবলৈ যত্ন কৰিছিল।
(ii) তেওঁ একে ভৌতিক আৰু ৰাসায়নিক ধর্মবিশিষ্ট মৌলসমূহক একেটা স্তম্ভতে স্থান দিবলৈ যত্ন কৰিছিল।
প্রশ্ন 7. সম্ভ্ৰান্ত গেছবোৰক এটা সুকীয়া বৰ্গত কিয় স্থান দিয়া হৈছে? [HSLC 2018]
উত্তৰ: কাৰণ, সম্ভ্ৰান্ত গেছসমূহৰ পৰমাণুৰ বহিৰ্তম কক্ষ ইলেক্ট্রনেৰে পূৰ্ণ হৈ থাকে, যাৰ বাবে ইহঁতে সুস্থিৰ ইলেক্ট্রনীয় বিন্যাস লাভ কৰে। ইয়াৰ বাবে আটাইবোৰ সম্ভ্ৰান্ত গেছে ৰাসায়নিকভাৱে নিষ্ক্রিয়তা দেখুৱায় !
প্রশ্ন ৪. আধুনিক পর্যাবৃত্ত তালিকাই মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকাত থকা আসোৱাহবোৰ কিদৰে দূৰ কৰিছিল ? [HSLC 2020]
উত্তৰ : (i) আধুনিক পর্যাবৃত্ত তালিকাত হাইড্ৰ’জেনক এক নির্দিষ্ট স্থান দিব পৰা গৈছিল। ইলেক্ট্ৰনীয় বিন্যাসৰ সাদৃশ্যৰ ওপৰত নিৰ্ভৰ কৰি হাইড্ৰ’জেনক প্ৰথম বৰ্গত এলকালি ধাতুসমূহৰ লগত স্থান দিয়া হৈছে।
(ii) আধুনিক পর্যাবৃত্ত তালিকাত সমস্থানিকবোৰে কোনো সমস্যাৰ সৃষ্টি কৰা নাছিল। কাৰণ একেটা মৌলৰ সমস্থানিকবোৰৰ পাৰমাণৱিক ভৰ বেলেগ বেলেগ যদিও, সিহঁতৰ পাৰমাণৱিক সংখ্যা আৰু ৰাসায়নিক ধৰ্মবোৰ একে।
(iii) যিহেতু আধুনিক পর্যাবৃত্ত তালিকাত এটা মৌলৰ পৰা পৰৱৰ্তী মৌলটোলৈ যাওঁতে পাৰমাণৱিক সংখ্যাৰ বৃদ্ধি সুষমভাৱে ঘটে, সেয়েহে দুটা মৌলৰ মাজত ভৱিষ্যতে কিমানটা নতুন মৌল আৱিষ্কৃত হ’ব, তাৰ সঠিক পূর্বানুমান কৰাটো সম্ভৱপৰ হৈছিল।
প্রশ্ন 9. মেগনেছিয়ামৰ দৰে ৰাসায়নিক বিক্রিয়া দেখুৱাব বুলি ভবা দুটা মৌলৰ নাম লিখা। তোমাৰ এই বাছনিৰ ভিত্তি কি ?
উত্তৰঃ বেৰিলিয়াম আৰু কেলছিয়াম।
এই বাছনিৰ ভিত্তি হ’ল— বেৰিলিয়াম আৰু কেলছিয়ামৰ পৰমাণুৰ বহিৰতম কক্ষত মেগনেছিয়ামৰ পৰমাণুত থকাৰ দৰে একে সংখ্যক ইলেক্ট্রন আছে। এই তিনিওটা মৌলৰ ইলেক্ট্ৰনীয় বিন্যাসবোৰ হ’ল—
মেগনেছিয়াম (12) = 2.8.2
বেৰিলিয়াম (4) = 2.2
কেলছিয়াম (20) = 2.8.8.2
প্রশ্ন 10. নাম লিখা—
(a) বহিৰতম কক্ষত এটাকৈ ইলেক্ট্রন থকা তিনিটা মৌলৰ।
উত্তৰ : লিথিয়াম, ছ’ডিয়াম আৰু পটাছিয়াম।
(b) বহিৰতম কক্ষত দুটাকৈ ইলেক্ট্রন থকা দুটা মৌলৰ।
উত্তৰঃ বেৰিলিয়াম আৰু মেগনেছিয়াম।
(c) পৰিপূৰ্ণ বৰিৰ্হতম কক্ষ থকা তিনিটা মৌলৰ৷
উত্তৰ: হিলিয়াম, নিয়ন আৰু আৰ্গন।
প্রশ্ন 11. (a) লিথিয়াম, ছ’ডিয়াম, পটাছিয়াম— এই আটাইকেইটা ধাতু। ইহঁতে পানীৰ সৈতে বিক্ৰিয়া কৰি হাইড্ৰ’জেন গেছ মুক্ত কৰে। এই মৌলকেইটাৰ পৰমাণুৰ কিবা সাদৃশ্য আছেনে? [HSLC 2019]
উত্তৰ: এই মৌলকেইটাৰ পৰমাণুৰ বহিৰতম কক্ষত এটাকৈ ইলেক্ট্রন আছে।
(b) হিলিয়াম এটা নিষ্ক্রিয় গেছ আৰু নিয়নো এটা প্রায় নিষ্ক্রিয় গেছ। ইহঁতৰ পৰমাণুবোৰৰ মাজত কি মিল থকা দেখা যায় ?
উত্তৰ : ইহঁতৰ পৰমাণুৰ বহিৰতম কক্ষ ইলেক্ট্রনেৰে পৰিপূৰ্ণ হৈ থাকে।
প্রশ্ন 12. আধুনিক পর্যাবৃত্ত তালিকাত থকা প্রথম দহোটা মৌলৰ ভিতৰত কোনকেইটা ধাতু?
উত্তৰঃ লিথিয়াম আৰু বেৰিলিয়াম।
প্রশ্ন 13. পর্যাবৃত্ত তালিকাত স্থান বিবেচনা কৰি তলৰ মৌলকেইটাৰ কোনটো আটাইতকৈ বেছি ধাতৱধৰ্মী হ’ব বুলি অনুমান কৰিবা ?
Ga, Ge, As, Se, Be
উত্তৰ : Be
অনুশীলনীৰ প্ৰশ্নোত্তৰ
প্রশ্ন 1. পর্যাবৃত্ত তালিকাৰ পৰ্যায়বোৰত বাঁওফালৰ পৰা সোঁফাললৈ যাওঁতে ঘটা পৰিৱৰ্তনৰ প্ৰকৃতিৰ ওপৰত আগবঢ়োৱা তলৰ উক্তিসমূহৰ কোনটো উক্তি শুদ্ধ নহয় ? [HSLC 2018]
(a) মৌলবোৰ কম ধাতৱধৰ্মী হৈ পৰে।
(b) যোজক ইলেক্ট্রনৰ সংখ্যা বাঢ়ে।
(c) পৰমাণুবোৰে সিহঁতৰ যোজক ইলেক্ট্রন অধিক সহজে হেৰুৱায়।
(d) অক্সাইডবোৰ বেছি আম্লিক হৈ পৰে।
উত্তৰ: (c) পৰমাণুবোৰে সিহঁতৰ যোজক ইলেক্ট্রন অধিক সহজে হেৰুৱায়।
প্রশ্ন 2. মৌল X য়ে XCI2 সংকেতৰ ক্ল’ৰাইড গঠন কৰে। ই উচ্চ গলনাংকযুক্ত এটা গোটা পদার্থ। মৌল X তলৰ কোনটোৰে সৈতে একেটা বৰ্গতে থকাৰ সম্ভাৱনা সবাতোকৈ বেছি? [HSLC 2019]
(a) Na (b) Mg (c) Al (d) Si
উত্তৰ : (b) Mg
প্রশ্ন 3. কোনটো মৌলৰ আছে——
(a) ইলেক্ট্ৰনৰ পূৰ্ণ দুটা কক্ষ? [HSLC 2017]
উত্তৰ: নিয়নৰ (2.8 )।
(b) 2.8.2 ইলেক্ট্রনীয় বিন্যাস?
উত্তৰ: মেগনেছিয়ামৰ।
(c) যোজক কক্ষত চাৰিটা ইলেক্ট্ৰনেৰে সৈতে মুঠ তিনিটা কক্ষ ? [HSLC 2017]
উত্তৰঃ ছিলিকনৰ (2.8.4)
(d) যোজক কক্ষত তিনিটা ইলেক্ট্রনেৰে সৈতে মুঠ দুটা কক্ষ ?
উত্তৰ : ব’ৰণৰ (2.3)
(e) দ্বিতীয় কক্ষত প্রথম কক্ষৰ দুগুণ ইলেক্ট্রন? [HSLC 2019]
উত্তৰ: কাৰ্বনৰ (2.4)।
প্রশ্ন 4. (a) পর্যাবৃত্ত তালিকাত ব’ৰণৰ সৈতে একেটা স্তম্ভতে থকা মৌলবোৰৰ কি কি সাধাৰণ ধৰ্ম আছে?
উত্তৰ: এই আটাইবোৰ মৌলৰে পৰমাণুৰ বহিৰতম কক্ষত তিনিটাকৈ ইলেক্ট্রন আছে আৰু ইহঁতৰ যোজ্যতা তিনি। ইহঁতে হাইড্ৰ’জেনৰ সৈতে বিক্রিয়া নকৰে।
(b) পর্যাবৃত্ত তালিকাত ফ্ল’ৰিণৰ সৈতে একেটা স্তম্ভতে থকা মৌলবোৰৰ কি কি সাধাৰণ ধৰ্ম আছে?
উত্তৰ: এই আটাইবোৰ মৌলৰে পৰমাণুৰ বহিৰতম কক্ষত সাতটাকৈ ইলেক্ট্রন আছে আৰু ইহঁত আটাইৰে যোজ্যতা এক। ইহঁতে প্রত্যক্ষভাৱে হাইড্ৰ’জেনৰ লগত বিক্ৰিয়া কৰি যৌগ উৎপন্ন কৰে যি পানীত দ্ৰৱীভূত হৈ এচিডলৈ ৰূপান্তৰিত হয়। (যেনে –– HE, HCI, HBr, HI এচিড।)।
প্রশ্ন 5. এটা পৰমাণুৰ ইলেক্ট্ৰনীয় বিন্যাস হ’ল – 2. 8. 7
(a) এই মৌলটোৰ পাৰমাণৱিক সংখ্যা কি ? [HSLC 2019]
উত্তৰ : 17
(b) তলৰ মৌলবোৰৰ কোনটোৰ সৈতে ইয়াৰ ৰাসায়নিক সাদৃশ্য থাকিব? (বন্ধনীৰ ভিতৰত পাৰমাণৱিক সংখ্যাবোৰ দিয়া আছে।) [HSLC 2017, 2020]
N(7), F(9), P(15), Ar ( 18 )
উত্তৰঃ F(9)
প্রশ্ন 6. পর্যাবৃত্ত তালিকাত তিনিটা মৌল A, B আৰু C ৰ স্থানসমূহ তলত দেখুওৱা হৈছে।
16 বর্গ 17 বর্গ
——- ——-
——- A
——- ——-
B C
(a) মৌল A ধাতু নে অধাতু?
(b) C মৌলটো A তকৈ বেছি সক্রিয়নে কম সক্রিয় ?
(c) C মৌলটো আকাৰত Bতকৈ ডাঙৰ নে সক।
(d) মৌল A এ কেনে ধৰণৰ আয়ন, কেটায়ন বা এনায়ন গঠন কৰিব ?
[HSLC 2016,2019]
উত্তৰ : (a) অধাতু।
(b) কম সক্রিয়
(c) সৰু ।
(d) এনায়ন।
প্রশ্ন 7. নাইট্ৰ’জেন (পাৰমাণৱিক সংখ্যা 7) আৰু ফছফ’ৰাহু (পাৰমাণৱিক সংখ্যা 15) পৰ্যাবৃত্ত তালিকাৰ বৰ্গ 15 ত থাকে। এই মৌল দুটাৰ ইলেক্ট্রনীয় বিন্যাস লিখা। ইহঁতৰ কোনটো বেছি বিদ্যুৎ ঋণাত্মক হ’ব আৰু কিয় ? [HSLC 2015, 2018]
উত্তৰ : নাইট্র’জেন (7) = 2.5
ফছফৰাছ (15) = 2.8.5
ইহঁতৰ ভিতৰত নাইট্ৰ’জেন বেছি বিদ্যুৎ ঋণাত্মক হ’ব। কাৰণ 15 তম বৰ্গত ফছফৰাছ নাইট্ৰ’জেনৰ তলত থাকে। আমি জানো যে আধুনিক পর্যাবৃত্ত তালিকাত বর্গ এটাত ওপৰৰ পৰা তলফাললৈ গ’লে মৌলবোৰৰ পাৰমাণৱিক আকাৰৰ বৃদ্ধি ঘটে। ইয়াৰ ফলত পৰমাণুৰ নিউক্লিয়াছৰ পৰা বহিৰতম কক্ষলৈ দূৰত্ব বাঢ়ে আৰু সেয়ে বহিৰতম কক্ষৰ প্ৰতি নিউক্লিয়াছৰ আকৰ্ষণ ক্রমে কমি যায়। এইবাবে মৌলসমূহৰ পৰমাণুৰ ইলেক্ট্রন গ্ৰহণ কৰাৰ প্ৰৱণতা ক্ৰমে কমি যায়। অর্থাৎ মৌলবোৰৰ বিদ্যুৎ ঋণাত্মক গুণ ক্ৰমে কমি যায়। এইবাবে 15 তম বৰ্গত নাইট্ৰ’জেন আৰু ফছফ’ৰাছৰ ভিতৰত নাইট্ৰ’জেন বেছি বিদ্যুৎ ঋণাত্মক।
প্রশ্ন ৪. পৰমাণু এটাৰ ইলেক্ট্রনীয় বিন্যাস আধুনিক পর্যাবৃত্ত তালিকাত তাৰ স্থানৰ সৈতে কিদৰে জড়িত হৈ আছে?
উত্তৰ: পৰমাণু এটাৰ ইলেক্ট্ৰনীয় বিন্যাসৰ পৰা পৰমাণুটোত থকা মুঠ কক্ষৰ সংখ্যা জনা যায়। আকৌ পৰমাণু এটাৰ কক্ষৰ সংখ্যাই আধুনিক পর্যাবৃত্ত তালিকাত ইয়াৰ পৰ্যায় সংখ্যা দিয়ে। উদাহৰণ স্বৰূপে, ছ’ডিয়ামৰ ইলেক্ট্ৰনীয় বিন্যাস 2.8.1; সেয়েহেই আধুনিক পর্যাবৃত্ত তালিকাত তৃতীয় পর্যায়ত থাকিব৷
তেনেদৰে পৰমাণু এটাৰ বহিৰতম কক্ষত এটা বা দুটা ইলেক্ট্রন থাকিলে সিহঁত পর্যাবৃত্ত তালিকাত ক্ৰমে প্ৰথম আৰু দ্বিতীয় বৰ্গত থাকিব। উদাহৰণস্বৰূপে, ছ’ডিয়াম (2.8.1) প্রথমবৰ্গত আৰু মেগনেছিয়াম (2.8.2) দ্বিতীয়বর্গত থাকিব।
আকৌ পৰমাণুটোৰ বহিৰতম কক্ষত থকা ইলেক্ট্রন সংখ্যা 3, 4, 5, 6, 7 বা 8 হ’লে এই সংখ্যাটোৰ লগত 10 যোগ কৰি পোৱা সংখ্যাটোৱে মৌলটোৰ বৰ্গ সংখ্যা দিব। উদাহৰণস্বৰূপে, এলুমিনিয়াম (2.8.3) 13 তম বৰ্গত আৰু আৰ্গন (2.8.8) 18 তম বর্গত থাকিব।
প্রশ্ন 9. আধুনিক পর্যাবৃত্ত তালিকাত কেলছিয়াম (পাৰমাণৱিক সংখ্যা 20 ) 12, 19, 21 আৰু 38 পাৰমাণৱিক সংখ্যাবিশিষ্ট মৌলকেইটাৰ দ্বাৰা পৰিৱেষ্টিত হৈ আছে। এই কেইটাৰ কাৰ কাৰ ভৌতিক আৰু ৰাসায়নিক ধর্মসমূহ কেলছিয়ামৰ সৈতে মিলে?
উত্তৰ: 12 আৰু 38 পাৰমাণৱিক সংখ্যাবিশিষ্ট মৌলকেইটাৰ ।
প্রশ্ন 10. মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকা আৰু আধুনিক পর্যাবৃত্ত তালিকাৰ মৌলৰ শ্ৰেণীবিভাজনৰ তুলনা কৰা।
উত্তৰ:
| মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকা | আধুনিক পর্যাবৃত্ত তালিকা |
| (i) মৌলসমূহক সিহঁতৰ পাৰমাণৱিক ভৰৰ বৰ্ধিত ক্ৰমত সজ্জিত কৰা হৈছিল। (ii) ছয়টা পর্যায় আৰু আঠটা বৰ্গ আছে। (iii) সংক্রমণশীল মৌলসমূহক একে-লগে একেটা বৰ্গতে (VIII বর্গ) স্থান দিয়া হৈছে। | (i) মৌলসমূহক সিহঁতৰ পাৰমাণৱিক সংখ্যাৰ বৰ্ধিত ক্ৰমত সজ্জিত কৰা হৈছিল। (ii) সাতটা পৰ্যায় আৰু ওঠৰটা বৰ্গ আছে। (iii) সংক্রমণশীল মৌলবোৰক পৃথক পৃথক বৰ্গত স্থান দিয়া হৈছে। |
অতিৰিক্ত প্রশ্নোত্তৰ
অতি চমু প্রশ্নোত্তৰ
প্রশ্ন 1. মৌলসমূহৰ শ্ৰেণীবিভাজন কৰাৰ প্ৰয়োজনীয়তা কি? [HSLC 2022]
উত্তৰ: বর্তমানে আমি 118 টা মৌলৰ বিষয়ে জানো। এই বৃহৎ সংখ্যক মৌলৰ প্ৰতিটোকে ব্যক্তিগতভাৱে অধ্যয়ন কৰাটো কষ্টসাধ্য। ইয়াৰ সলনি ধৰ্মৰ সাদৃশ্যৰ ওপৰত ভিত্তি কৰি মৌলসমূহক কিছুমান গোষ্ঠীত বিভক্ত কৰিলে, এই গোষ্ঠীসমূহৰ অধ্যয়নৰ দ্বাৰা মৌলসমূহক জানিবলৈ বেছি সহজসাধ্য হয়। এইবাবে মৌলসমূহৰ শ্রেণীবিভাজন কৰাটো প্ৰয়োজনীয়।
প্রশ্ন 2. ড’বাৰেইনাৰৰ ট্ৰায়াড কি?
উত্তৰ: জার্মান ৰসায়নবিদ ডবাৰেইনাৰে এক ধৰ্মবিশিষ্ট মৌলবোৰক একো একোটা গোটত সজাবলৈ যত্ন কৰিছিল। তেওঁ তিনিটাকৈ মৌল থকা কেইটামান গোট চিনাক্ত কৰিছিল। এই গোটসমূহক ড’বাৱেইনাৰৰ ট্ৰায়াড বা ত্ৰিক বোলা হৈছিল।
প্রশ্ন 3. ড’বাৰেইনাৰৰ ট্ৰায়াডৰ তিনিটা উদাহৰণ দিয়া।
উত্তৰঃ
Li Ca Cl
Na Sr Br
K Ba I
প্রশ্ন 4, ড’বাৰেইনাৰৰ ট্ৰায়াড একোটাৰ এক উল্লেখনীয় বৈশিষ্ট্য লিখা।
উত্তৰঃ ট্রায়াড এটাৰ মৌল তিনিটাক সিহঁতৰ পাৰমাণৱিক ভৰৰ বৰ্দ্ধিত ক্ৰমত সজালে মাজৰ মৌলটোৰ পাৰমাণৱিক ভৰ আন দুটা মৌলৰ পাৰমাণৱিক ভৰৰ গড় মানৰ প্ৰায় সমান হয়।
প্রশ্ন 5. নিউলেণ্ডছৰ অষ্টক সূত্ৰটো কি? [HSLC 2020]
উত্তৰ : ইংৰাজী বিজ্ঞানী জন নিউলেণ্ডছে সেই সময়লৈকে আৱিষ্কৃত 56 টা মৌলক সিহঁতৰ পাৰমাণৱিক ভৰৰ বৰ্ধিত ক্ৰমত সজাইছিল। এনেদৰে সজাওঁতে তেওঁ প্ৰতিটো অষ্টম মৌলৰ ধৰ্ম প্ৰথমটো মৌলৰ সৈতে একে ধৰণৰ হোৱা লক্ষ্য কৰিছিল। এইটোক তেওঁ সংগীতৰ অষ্টকৰ লগত তুলনা কৰিছিল। ইয়াক নিউলেণ্ডছৰ অষ্টক সূত্ৰ নামেৰে জনা যায়।
প্রশ্ন 6. মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকা কি?
উত্তৰ : ৰুছ ৰসায়ন বিজ্ঞানী মেণ্ডেলিভে তেওঁৰ সময়লৈকে জনা যোৱা 63 টা মৌলক সিহঁতৰ পাৰমাণৱিক ভৰৰ বৰ্ধিত ক্ৰমত সজাইছিল। এনেদৰে সজাওঁতে দেখা গৈছিল যে এক নিৰ্দিষ্ট অন্তৰালৰ মূৰে মূৰে একে ধৰণৰ ভৌতিক আৰু ৰাসায়নিক ধৰ্ম প্ৰদৰ্শন কৰা মৌলবোৰৰ পুনৰাবৃত্তি ঘটে। এনেদৰে প্ৰস্তুত কৰি উলিওৱা মৌলৰ তালিকাখনক মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকা বোলে।
প্রশ্ন 7, মেণ্ডেলিভে তেওঁৰ তালিকাখনত মৌলবোৰক কিহৰ ভিত্তিত সজাইছিল ? [HSLC 2022]
উত্তৰঃ মৌলবোৰৰ এক মৌলিক ধৰ্ম পাৰমাণৱিক ভৰ আৰু সিহঁতৰ ৰাসায়নিক ধৰ্মৰ সাদৃশ্যৰ ভিত্তিত।
প্রশ্ন ৪. মৌলসমূহৰ ৰাসায়নিক ধৰ্মৰ পৰীক্ষাৰ বাবে মেণ্ডেলিভে কিহৰ ওপৰত গুৰুত্ব দিছিল ?
উত্তৰঃ মৌলবোৰে অক্সিজেন আৰু হাইড্ৰ’জেনৰ সৈতে গঠন কৰা যৌগবোৰৰ ওপৰত।
প্রশ্ন 9. ৰাসায়নিক ধর্মসমূহৰ ভিতৰত মৌলবোৰৰ অক্সিজেন আৰু হাইড্ৰ’জেনৰ সৈতে গঠন কৰা যৌগবোৰৰ ওপৰত মেণ্ডেলিভে কিয় গুৰুত্ব দিছিল?
উত্তৰ: কাৰণ ইহঁত যথেষ্ট সক্রিয় মৌল আৰু অধিকাংশ মৌলৰেই সৈতে ইহঁতে যৌগ গঠন কৰে।
প্রশ্ন 10. মেণ্ডেলিভে মৌল এটাক শ্রেণীভুক্ত কৰিবলৈ মৌলটোৱে গঠন কৰা কেনে ধৰণৰ যৌগৰ সংকেতক মৌলটোৰ অন্যতম মূল ধর্ম হিচাপে বিবেচনা কৰিছিল ?
উত্তৰ: মৌলটোৱে গঠন কৰা হাইড্ৰাইড আৰু অক্সাইডসমূহৰ সংকেতক।
প্রশ্ন 11. মেণ্ডেলিভৰ পৰ্যাবৃত্ত সূত্ৰটো লিখা।
উত্তৰ: মৌলবোৰৰ ধৰ্মবোৰ সিহঁতৰ পাৰমাণৱিক ভৰৰ পৰ্যায়ক্রমে সলনি হয়।
প্রশ্ন 12. মেণ্ডেলিভে তেওঁৰ পৰ্যাবৃত্ত তালিকাখনত কিছুমান খালী ঠাই এৰি গৈছিল ৷ ইয়াক তুমি তালিকাখনৰ এক বিসংগতি বুলি ভাবানে? কাৰণ দর্শোৱা।
উত্তৰ: নাভাবোঁ । কাৰণ এই খালী ঠাইবোৰত সেই সময়লৈকে আৱিষ্কৃত নোহোৱা কিছুমান মৌলৰ অৱস্থিতিৰ বিষয়ে মেণ্ডেলিভে সঠিকভাৱে ভৱিষ্যতবাণী কৰিছিল।
প্রশ্ন 13. মেণ্ডেলিভে ক্রমে একা ব’ৰণ, একা-এলুমিনিয়াম আৰু একা-ছিলিকন নাম দিয়া মৌলসমূহক আৱিষ্কৃত হোৱাৰ পিছত কেনেদৰে নতুনকৈ নামকৰণ কৰা হৈছিল?
উত্তৰঃ (i) একা-ব’ৰণ — স্কেন্ডিয়াম
(ii) একা-এলুমিনিয়াম — গেলিয়াম
(iii) একা-ছিলিকন – জার্মেনিয়াম
প্রশ্ন 14. কোনগৰাকী বিজ্ঞানীয়ে পোন প্ৰথমবাৰৰ বাবে দেখুৱাইছিল যে মৌল এটাৰ পাৰমাণৱিক সংখ্যা তাৰ পাৰমাণৱিক ভৰতকৈ অধিকতৰ মৌলিক?
উত্তৰঃ হেনৰী ম’জলে নামৰ বিজ্ঞানীগৰাকীয়ে।
প্রশ্ন 15. আধুনিক পর্যাবৃত্ত সূত্ৰটো কি? [HSLC 2020]
উত্তৰঃ মৌলবোৰৰ ধৰ্মবোৰ সিহঁতৰ পাৰমাণৱিক সংখ্যাৰ পৰ্যায়ক্রমে সলনি হয়।
প্রশ্ন 16. আধুনিক পর্যাবৃত্ত তালিকা বুলিলে কি বুজা?
উত্তৰঃ মৌলবোৰক সিহঁতৰ পাৰমাণৱিক সংখ্যাৰ বৰ্ধিত ক্ৰমত সজ্জিত কৰিলে এক ভৌতিক আৰু ৰাসায়নিক ধর্মবিশিষ্ট মৌলবোৰৰ পুনৰাবৃত্তি ঘটে। এনেদৰে প্ৰস্তুত কৰা মৌলসমূহৰ তালিকাখনক আধুনিক পর্যাবৃত্ত তালিকা বোলে।
প্রশ্ন 17. আধুনিক পর্যাবৃত্ত তালিকাত বৰ্গ আৰু পৰ্যায় বুলিলে কি বুজা?
উত্তৰঃ আধুনিক পর্যাবৃত্ত তালিকাত 18 টা থিয় স্তম্ভ আৰু 7 টা আনুভূমিক শাৰী আছে। এইবোৰক ক্ৰমে বৰ্গ আৰু পৰ্যায় বোলে।
প্রশ্ন 18. আধুনিক পর্যাবৃত্ত তালিকাত প্রথম, দ্বিতীয়, তৃতীয় আৰু চতুর্থ পর্যায়ত কিমানটাকৈ মৌল আছে?
উত্তৰঃ প্রথম, দ্বিতীয়, তৃতীয় আৰু চতুর্থ পর্যায়ত ক্ৰমে 2 টা, ৪ টা, ৪ টা আৰু 18 টা মৌল আছে।
প্রশ্ন 19. তলৰ মৌল দুটাৰ যোজ্যতা নির্ণয় কৰা।
(i) মেগনেছিয়াম (12) (ii) ছালফাৰ (16)
উত্তৰঃ (i) মেগনেছিয়াম (2.8.2) যোজ্যতা = 2
(ii) ছালফাৰ (2.8.6) যোজ্যতা = 2
প্রশ্ন 20. পর্যায় এটাত বাঁওফালৰ পৰা সোঁফাললৈ গ’লে যোজ্যতা কিদৰে পৰিৱৰ্তিত হয়?
উত্তৰঃ প্রথমে 1 ৰ পৰা 4 লৈ বৃদ্ধি হৈ পিছত 4 ৰ পৰা শূন্যলৈ হ্রাস পায়। [প্রথম তিনিটা পৰ্যায়ৰ ক্ষেত্ৰত]
প্রশ্ন 21. বৰ্গ এটাত ওপৰৰ পৰা তললৈ আহিলে যোজ্যতা কিদৰে পৰিৱৰ্তিত হয় ?
উত্তৰঃ বৰ্গ এটাত মৌলবোৰৰ যোজ্যতা একে থাকে।
প্রশ্ন 22. পাৰামণৱিক ব্যাসার্ধ বা আকাৰ কাক বোলে?
উত্তৰঃ মৌলৰ পৰমাণু এটাৰ নিউক্লিয়াছৰ কেন্দ্ৰ আৰু বহিৰতম কক্ষৰ মাজৰ দূৰত্বক মৌলটোৰ পাৰমাণৱিক ব্যাসার্ধ বোলে। মৌলৰ পাৰমাণৱিক ব্যাসার্ধই মৌলটোৰ পাৰমাণৱিক আকাৰ দিয়ে।
প্রশ্ন 23. পর্যায় এটাত বাঁওফালৰ পৰা সোঁফাললৈ গ’লে কিদৰে পাৰামাণৱিক ব্যাসার্ধৰ পৰিৱৰ্তন ঘটে?
উত্তৰঃ ক্রমান্বয়ে হ্রাস পায়।
প্রশ্ন 24. বর্গ এটাত ওপৰৰ পৰা তললৈ গ’লে পাৰমাণৱিক আকাৰৰ পৰিৱৰ্তন কেনেদৰে ঘটে ?
উত্তৰঃ ক্ৰমান্বয়ে বৃদ্ধি পায়।
প্রশ্ন 25. পর্যাবৃত্ত তালিকাৰ কোনফালে ধাতু আৰু কোনফালে অধাতুবোৰ পোৱা যায়?
উত্তৰঃ পর্যাবৃত্ত তালিকাত ধাতুসমূহ বাঁওফালে আৰু অধাতুবোৰ সোঁফালে পোৱা যায়।
প্রশ্ন 26. তৃতীয় পৰ্যায়ৰ মৌলবোৰ পৰীক্ষা কৰা আৰু ইহঁতক ধাতু আৰু অধাতৃ হিচাপে শ্রেণীবিভাজন কৰা।
উত্তৰঃ ধাতু – -ছ’ডিয়াম, মেগনেছিয়াম, এলুমিনিয়াম।
অধাতু – ফছফৰাছ, ছালফাৰ, ক্লবিন, আর্গন।
প্রশ্ন 27. পর্যায় এটাত মৌলবোৰৰ ধাতবীয় ধর্ম (ইলেক্ট্রন হেৰুওৱাৰ প্ৰৱণতা) কিদৰে ক্ৰম পৰিবৰ্তিত হয়?
উত্তৰঃ ক্রমান্বয়ে কমে।
প্রশ্ন 28. বর্গ এটাত মৌলবোৰৰ ধাতবীয় ধর্ম (ইলেক্ট্রন হেৰুওৱাৰ প্ৰৱণতা) কিদৰে ক্রম পৰিৱৰ্তিত হয়?
উত্তৰঃ ক্রমান্বয়ে বাঢ়ে।
প্রশ্ন 29. পর্যায় এটাত মৌলবোৰৰ অধাতত্ত্বীয় ধৰ্ম (ইলেক্ট্রন লাভ কৰাৰ প্ৰৱণতা) কিদৰে সলনি হয় ?
উত্তৰঃ ক্রমান্বয়ে বাঢ়ে।
প্রশ্ন 30. বৰ্গ এটাত মৌলবোৰৰ অধাতত্ত্বীয় ধৰ্ম (ইলেক্ট্রন লাভ কৰাৰ প্ৰৱণতা) কিদৰে সলনি হয় ?
উত্তৰঃ ক্রমান্বয়ে কমে।
প্রশ্ন 31. পর্যায় এটাত মৌলৰ অক্সাইডসমূহৰ প্ৰকৃতিৰ কিদৰে ক্ৰম পৰিৱৰ্তন ঘটে ?
উত্তৰঃ অক্সাইডসমূহৰ ক্ষাৰকীয় গুণ ক্ৰমে কমে আৰু আম্লিক গুণ ক্রমান্বয়ে বাঢ়ে।
প্রশ্ন 32. বৰ্গ এটাত মৌলৰ অক্সাইডসমূহৰ প্ৰকৃতিৰ কিদৰে ক্ৰম পৰিৱৰ্তন ঘটে?
উত্তৰঃ অক্সাইডসমূহৰ ক্ষাৰকীয় গুণ ক্ৰমে বাঢ়ে আৰু আম্লিক গুণ ক্ৰমে কমে।
প্রশ্ন 33. তলৰ মৌলবোৰৰ ইলেক্ট্রনীয় বিন্যাস লিখি পর্যাবৃত্ত তালিকাত সিহঁতৰ পৰ্যায়সংখ্যা আৰু বৰ্গসংখ্যা নির্ণয় কৰা।
(a) কেলছিয়াম (b) ফ্লৰিণ (c) লিথিয়াম।
উত্তৰঃ
(a) কেলছিয়াম — 2.8.8.2
পর্যায় সংখ্যা = 4 [ কক্ষৰ সংখ্যা =4]
বর্গ সংখ্যা = 2 [ যোজক ইলেক্ট্রন সংখ্যা = 2]
(b) ফ্লৰিণ – 2.7
পর্যায়সংখ্যা = 2 [ কক্ষৰ সংখ্যা = 2]
বর্গ সংখ্যা = 17 [যোজক ইলেক্ট্রন সংখ্যা 7 + 10 = 17]
(c) লিথিয়াম – 2.1
পর্যায় সংখ্যা = 2 [ কক্ষ সংখ্যা = 2]
বৰ্গৰ সংখ্যা = 1 [যোজক ইলেক্ট্রন সংখ্যা =1]
প্রশ্ন 34. আধুনিক পর্যাবৃত্ত তালিকাত হাইড্ৰ’জেনক ক’ত স্থান দিয়া উচিত বুলি ভাবা ? ইয়াৰ ভিত্তি কি?
উত্তৰঃ প্রথম পৰ্যায়ত, প্ৰথম বৰ্গত। প্রথম বৰ্গৰ আন মৌলসমূহৰ দৰে একে বহির্কক্ষীয় ইলেক্ট্রনীয় বিন্যাস থকাৰ ভিত্তিত হাইড্ৰ’জেনক এলকালি ধাতুসমূহৰ লগত প্ৰথম বৰ্গত স্থান দিয়া হয় । আকৌ আটাইতকৈ কম পাৰমাণৱিক সংখ্যা (1) ৰ বাবে ই পর্যাবৃত্ত তালিকাৰ প্রথমতে প্রথম পর্যায়ত স্থান পায়।
প্রশ্ন 35. কোনটো মৌলৰ ইলেক্ট্রনীয় বিন্যাস 2.8.3? [HSLC 2017]
উত্তৰঃ এলুমিনিয়ামৰ
চমু প্রশ্নোত্তৰ
প্রশ্ন 1. মেগুেলিভে কেনেদৰে তেওঁৰ পৰ্যাবৃত্ত তালিকাখন যুগুত কৰিছিল ?
উত্তৰঃ মেণ্ডেলিভৰ সময়লৈকে 63 টা মৌলৰ বিষয়ে জনা গৈছিল। তেওঁ মৌলসমূহৰ পাৰমাণৱিক ভৰৰ সৈতে সিহঁতৰ ভৌতিক আৰু ৰাসায়নিক ধৰ্মৰ সম্পৰ্ক পৰীক্ষা কৰি চাইছিল। ৰাসায়নিক ধর্মসমূহৰ ভিতৰত মৌলবোৰৰ অক্সিজেন আৰু হাইড্ৰ’জেনৰ সৈতে গঠন কৰা যৌগবোৰৰ ওপৰত মেণ্ডেলিভে গুৰুত্ব দিছিল। তেওঁ 63 খন কার্ড লৈ মৌল একোটাৰ ধৰ্মবোৰ একোখন কাৰ্ডত লিখি গৈছিল। অনুৰূপ ধৰ্ম প্ৰদৰ্শন কৰা মৌলসমূহ ভাগে ভাগে বাছি লৈ সেইমতে কাৰ্ডবোৰ বেৰত গাঁঠি গৈছিল। তেওঁ লক্ষ্য কৰিছিল যে মৌলবোৰৰ অধিকাংশই পর্যাবৃত্ত তালিকা এখনত ঠাই পাইছিল আৰু সিহঁত পাৰামাণৱিক ভৰৰ বৰ্ধিত ক্ৰমত সজ্জিত হৈছিল। এইটোও দেখা গৈছিল যে এক নিৰ্দিষ্ট অন্তৰালৰ মূৰে মূৰে একে ভৌতিক আৰু ৰাসায়নিক ধৰ্ম দেখুওৱা মৌলবোৰৰ পুনৰাবৃত্তি ঘটে।
প্রশ্ন 2. মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকাৰ সফলতাসমূহ লিখা।
উত্তৰঃ (i) মেণ্ডেলিভে তেওঁৰ তালিকাখনত কিছুমান । ঠাই এৰি গৈছিল। এই খালী ঠাইবোৰত সেই সময়লৈকে আৱিষ্কৃত নোহোৱা কিছুমান মৌলৰ অৱস্থিতিৰ বিষয়ে মেণ্ডেলিভে সঠিকভাৱে ভৱিষ্যদ্বাণী কৰিছিল। এই মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকাখন যে শুদ্ধ আৰু ব্যৱহাৰোপযোগী তাক নিশ্চিতভাৱে প্ৰমাণ কৰিছিল।
(ii) হিলিয়াম, নিয়ন, আর্গন আদিৰ দৰে সম্ভ্ৰান্ত গেছবোৰ অতিশয় নিষ্ক্রিয় আৰু বায়ুমণ্ডলত এইবোৰ নিচেই কম মাত্ৰাত থাকে বাবে এইবোৰ আৱিষ্কৃত হওঁতে বহু পলম হৈছিল। যেতিয়া আৱিষ্কৃত হ’ল, তেতিয়া ইহঁতক তালিকাখনত ইতিপূৰ্বে থকা ক্ৰমৰ কোনো সাল-সলনি নকৰাকৈ এটা নতুন বৰ্গত সংস্থাপিত কৰিব পৰা গৈছিল।
প্রশ্ন 3. মেণ্ডেলিভৰ শ্ৰেণীবিভাজনৰ সীমাবদ্ধতাবোৰ লিখা।
উত্তৰঃ (i) মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকাত হাইড্ৰ’জৈনক এক নিৰ্দিষ্ট স্থান দিব পৰা নগৈছিল।
(ii) মেণ্ডেলিভে মৌলৰ পৰ্যাবৃত্ত শ্রেণীবিভাজন কৰাৰ বহু পাছত সমস্থানিকবোৰ আৱিষ্কৃত হৈছিল৷ মৌল এটাৰ সমস্থানিকবোৰৰ ৰাসায়নিক ধর্মসমূহ একে হয়, কিন্তু সিহঁতৰ পাৰামাণৱিক ভৰবোৰ বেলেগ বেলেগ। সেয়েহে মৌলসমূহৰ সমস্থানিকবোৰে মেণ্ডেলিভৰ পর্যাবৃত্ত তালিকাৰ বাবে এক প্ৰত্যাহ্বানৰ সৃষ্টি কৰিছিল।
(iii) মেণ্ডেলিভৰ পৰ্যাবৃত্ত তালিকাৰ আন এটা সমস্যা আছিল— এটা মৌলৰ পৰা পাছৰ মৌলটোলৈ যাওঁতে মৌলবোৰৰ পাৰমাণৱিক ভৰৰ বৃদ্ধি সুষমভাৱে নঘটে। সেয়েহে দুটা মৌলৰ মাজত কিমানটা নতুন মৌল আৱিষ্কৃত হ’ব তাক পূর্বানুমান কৰাটো সম্ভৱ নহৈছিল।
প্রশ্ন 4. পর্যায় এটাত বাঁওফালৰ পৰা সোঁফাললৈ গ’লে মৌলবোৰৰ পাৰমাণৱিক আকাৰ (বা ব্যাসার্ধ) কমে কিয়?
উত্তৰঃ কাৰণ পৰ্যায় এটাত বাঁওফালৰ পৰা সোঁফাললৈ গ’লে মৌলসমূহৰ পাৰামাণৱিক সংখ্যাৰ বৃদ্ধি ঘটে। অর্থাৎ মৌলবোৰৰ পৰমাণুৰ নিউক্লিয়াছত এটাকৈ প্ৰট’নৰ সংখ্যাৰ বৃদ্ধি ঘটে। ই মৌলবোৰৰ পৰমাণুৰ নিউক্লীয় আধানৰ বৃদ্ধি ঘটায়। বৰ্ধিত নিউক্লীয় আধানে পৰমাণুৰ ইলেক্ট্রনবোৰক শক্তিশালীভাৱে আকৰ্ষণ কৰি নিউক্লিয়াছৰ বেছি ওচৰলৈ টানি আনে। এইবাবে পর্যায় এটাত মৌলবোৰৰ পাৰমাণৱিক আকাৰ ক্ৰমান্বয়ে কমে।
প্রশ্ন 5. বৰ্গ এটাত ওপৰৰ পৰা তললৈ আহিলে মৌলবোৰৰ পাৰমাণৱিক আকাৰৰ বৃদ্ধি ঘটে কিয় ?
উত্তৰঃ আধুনিক পর্যাবৃত্ত তালিকাত বৰ্গ এটাত তললৈ যোৱাৰ লগে লগে মৌল এটাৰ পৰমাণুত নতুন কক্ষ একোটা সংযোজিত হয়। ই পৰমাণুৰ নিউক্লিয়াছৰ পৰা বহিৰতম কক্ষৰ ইলেক্ট্ৰনলৈ দূৰত্ব বঢ়ায়। এইবাবে বৰ্গ এটাত তলফাললৈ গ’লে নিউক্লীয় আধান বঢ়া সত্ত্বেও মৌলবোৰৰ পাৰমাণৱিক আকাৰ বাঢ়ে।
প্রশ্ন 6. পর্যায় এটাত বাঁওফালৰ পৰা সোঁফাললৈ গ’লে মৌলবোৰৰ ধাতৱীয় ধৰ্ম কিয় কমে?
উত্তৰঃ আধুনিক পর্যাবৃত্ত তালিকাত পর্যায় এটাত বাঁওফালৰ পৰা সোঁফাললৈ গ’লে মৌলবোৰৰ পৰমাণুৰ নিউক্লীয় আধানৰ বৃদ্ধি ঘটে। ইয়াৰ ফলত পৰমাণুৰ নিউক্লিয়াছে ইলেক্ট্রনবোৰক অধিক শক্তিশালীভাৱে আকৰ্ষণ কৰিবলৈ ধৰে আৰু ইলেক্ট্ৰনবোৰকো নিউক্লিয়াছৰ বেছি ওচৰ চপাই আনে। ইয়াৰ বাবে পৰমাণুবোৰৰ ইলেক্ট্রন হেৰুওৱাৰ প্ৰৱণতা কমে। অর্থাৎ পর্যায় এটাত মৌলবোৰৰ ধাতৱীয় ধর্ম বা বিদ্যুৎ ধনাত্মক গুণ ক্রমান্বয়ে কমে।
প্রশ্ন 7. বৰ্গ এটাত তললৈ আহিলে মৌলবোৰৰ ধাতবীয় ধর্ম কিয় বাঢ়ে?
উত্তৰঃ আধুনিক পর্যাবৃত্ত তালিকাত বৰ্গ এটাত তলফাললৈ আহিলে মৌলসমূহৰ পৰমাণুত এটাকৈ নতুন কক্ষ সংযোজিত হোৱাৰ ফলত মৌলবোৰৰ পাৰমাণৱিক আকাৰ ক্রমান্বয়ে বাঢ়ে। ইয়াৰ ফলত মৌলবোৰৰ পৰমাণুৰ নিউক্লিয়াছৰ পৰা বহিৰতম কক্ষৰ ইলেক্ট্ৰনলৈ দূৰত্ব বাঢ়ে। ইয়াৰ বাবে বহিৰতম কক্ষৰ ইলেক্ট্ৰনৰ প্ৰতি নিউক্লিয়াছৰ আকৰ্ষণ ক্রমান্বয়ে কমে। সেয়েহে বৰ্গ এটাত তলফাললৈ গ’লে মৌলবোৰৰ পৰমাণুৰ ইলেক্ট্ৰন
হেৰুওৱাৰ প্ৰৱণতা বাঢ়ে। অর্থাৎ মৌলবোৰৰ ধাতৱীয় ধর্ম বা বিদ্যুৎ ধনাত্মক গুণ ক্রমান্বয়ে বাঢ়ে।
প্রশ্ন ৪. পর্যায় এটাত মৌলবোৰৰ অধাতত্ত্বীয় ধর্ম কিয় বাঢ়ে?
উত্তৰঃ আধুনিক পর্যাবৃত্ত তালিকাত পর্যায় এটাত বাঁওফালৰ পৰা সোঁফাললৈ গ’লে মৌলবোৰৰ পৰমাণুৰ নিউক্লীয় আধানৰ মান ক্রমান্বয়ে বাঢ়ে। ইয়াৰ বাবে মৌলবোৰৰ পৰমাণুৰ নিউক্লিয়াছে ইলেক্ট্রনসমূহক অধিক শক্তিশালীভাৱে আকৰ্ষণ কৰিবলৈ ধৰে। এই বৰ্ধিত আকর্ষণী বলৰ প্ৰভাৱত পৰমাণুবোৰে যোজক কক্ষত আন ইলেক্ট্রন গ্ৰহণ কৰিব পাৰে।এইবাবে পৰ্যায় এটাত সোঁফাললৈ গ’লে মৌলবোৰৰ ইলেক্ট্রন লাভ কৰাৰ প্ৰৱণতা অর্থাৎ সিহঁতৰ অধাতৱীয় ধৰ্ম বা বিদ্যুৎ ঋণাত্মক গুণ বাঢ়ে।
প্রশ্ন 9. বৰ্গ এটাত তললৈ আহিলে মৌলবোৰৰ অধাতত্ত্বীয় ধর্ম কিয় কমে?
উত্তৰঃ আধুনিক পর্যাবৃত্ত তালিকাত বৰ্গ এটাত তললৈ আহিলে মৌলবোৰৰ পাৰমাণৱিক আকাৰ বাঢ়ে। ইয়াৰ ফলত পৰমাণুৰ নিউক্লিয়াছৰ পৰা বহ্নিতম কক্ষলৈ দূৰত্ব বাঢ়ে। ইয়াৰ বাবে বহিৰতম কক্ষৰ প্ৰতি নিউক্লিয়াছৰ আকৰ্ষণ কমে। এই ক্রমহ্রাসমান আকর্ষণী বলৰ বাবে বৰ্গ এটাত তললৈ গ’লে মৌলবোৰৰ পৰমাণুৰ ইলেক্ট্রন গ্ৰহণ কৰাৰ প্ৰৱণতা কমে, অৰ্থাৎ অধাতৱীয় ধৰ্ম বা বিদ্যুৎ ঋণাত্মক গুণ কমে।
প্রশ্ন 10. ধাতুকল্প বা অর্ধধাতু কাক বোলে? ধাতুকল্পকেইটাৰ নাম লিখা।
উত্তৰঃ যিবিলাক মৌলই ধাতু আৰু অধাতু উভয়ৰে কিছুমান ধৰ্ম প্ৰদৰ্শন কৰে, সিহঁতক ধাতুকল্প বা অর্ধ-ধাতু বোলে।
যেনে – – ব’ৰণ, ছিলিকন, জার্মেনিয়াম, আর্জেনিক, এন্টিমনি, টেলুৰিয়াম আৰু পল’নিয়াম।
প্রশ্ন 11. তিনিটা মৌলৰ পাৰমাণৱিক সংখ্যা ক্রমে 4, 8, 101
(i) মৌলকেইটা চিনাক্ত কৰা।
(ii) মৌলকেইটাৰ ইলেক্ট্রনীয় বিন্যাস লিখা।
(iii) পর্যাবৃত্ত তালিকাত মৌলকেইটাৰ পৰ্যায় চিনাক্ত কৰা।
উত্তৰঃ (i) মৌলকেইটা হ’ল— বেৰিলিয়াম, অক্সিজেন, নিয়ন।
(ii) বেৰিলিয়াম (4) = 2.2
অক্সিজেন (8) = 2.6
নিয়ন (10) = 2.8
(iii) পর্যাবৃত্ত তালিকাত এই মৌলকেইটা দ্বিতীয় পর্যায়ত থাকিব।
প্রশ্ন 12. পর্যাবৃত্ত তালিকাৰ এটা অংশ তলত দেখুওৱা হ’ল :
| বর্গ পর্যায় | I | II | XVI | XVII | XVIII |
| 1 | B | D | C | ||
| 2 | E |
ওপৰৰ তালিকাৰ ওপৰত ভিত্তি কৰি তলৰ প্ৰশ্নবোৰৰ উত্তৰ লিখা :
(i) কোনটো মৌলই কেটায়ন গঠন কৰে?
(ii) কোনটো মৌলৰ পাৰমাণৱিক আকাৰ আটাইতকৈ কম?
(iii) কোনটো মৌলৰ ৰাসায়নিক ধর্ম মেগনেছিয়ামৰ (পাৰমাণৱিক সংখ্যা 12) ৰ সৈতে একে ধৰণৰ ? [HSLC 2015]
উত্তৰঃ (i) মৌল B য়ে।
(ii) মৌল C ৰ
(iii) মৌল B ৰ
প্রশ্ন 13. এটা মৌলৰ পৰমাণুৰ ইলেক্ট্রনীয় বিন্যাস 2.8.1
(i) মৌলটোৰ পাৰামাণৱিক সংখ্যা কিমান?
(ii) তলৰ মৌলবোৰৰ কোনটোৰ সৈতে ইয়াৰ ৰাসায়নিক সাদৃশ্য আছে? (বন্ধনীৰ ভিতৰত পাৰমাণৱিক সংখ্যাবোৰ দিয়া আছে)K(19), Cl(17), Mg (12), Ar ( 18 ) [HSLC 2016]
উত্তৰঃ (i) 11
(ii) K (19)
প্রশ্ন 14. যদি মৌল A আৰু B ৰ পাৰমাণৱিক সংখ্যা যথাক্রমে 12 আৰু 17।
(i) A আৰু B ৰ ইলেক্ট্রনীয় বিন্যাস লিখা।
(ii) A আৰু B ৰ মাজত কোন প্ৰকাৰৰ বান্ধনি গঠন হ’ব?
(iii) A আৰু B মাজত গঠন হোৱা যৌগটোৰ সংকেত লিখা। [HSLC 2017]
উত্তৰঃ (i) A (12) = 2.8.2
B (17) = 2.8.7
(ii) ইলেক্ট্র’যোজী বা আয়নীয় বান্ধনি।
(iii) AB2
প্রশ্ন 15. আধুনিক পর্যাবৃত্ত তালিকাৰ বৰ্গ 1 ৰ প্রথম তিনিটা মৌলৰ ইলেক্ট্রনীয় বিন্যাস লিখা। সিহঁতৰ ইলেক্ট্ৰনীয় বিন্যাসত কি সাদৃশ্য দেখা পাবা?
উত্তৰ: হাইড্ৰজেন (1) = 1
লিথিয়াম (3) = 2.1
ছ’ডিয়াম (11) = 2.8.1
ইহঁতৰ ইলেক্ট্ৰনীয় বিন্যাসবোৰৰ সাদৃশ্য এয়ে যে এই মৌলকেইটাৰ পৰমাণুত একে সংখ্যক যোজক ইলেক্ট্রন আছে (1 টাকৈ)।
প্রশ্ন 16. তিনিটা মৌল Na, Al আৰু P ৰ পাৰামাণৱিক সংখ্যাবোৰ ক্ৰমে 11, 13 আৰু 15। ইহঁতৰ প্ৰতিটোৰে ইলেক্ট্ৰনীয় বিন্যাস লিখা। ইহঁত পর্যাবৃত্ত তালিকাৰ কোনটো পর্যায়ত থাকিব?
উত্তৰ : Na(11) = 2.8.1
Al (13) = 2.8.3
P(15) = 2.8.5
ইহঁত পর্যাবৃত্ত তালিকাৰ তৃতীয় পৰ্যায়ত থাকিব।
প্রশ্ন 17. ইলেক্ট্রনীয় বিন্যাসৰ পৰা মৌল এটাৰ যোজ্যতা কেনেকৈ গণনা কৰিবা? মেগনেছিয়াম (12) আৰু ছালফাৰ (16) ৰ যোজ্যতা কিমান?
উত্তৰঃ মৌল এটাৰ পৰমাণুৰ বহিৰতম কক্ষৰ ইলেক্ট্ৰনৰ সংখ্যাই মৌলটোৰ যোজ্যতা নিৰ্ণয় কৰাত সহায় । কাৰণ, মৌল এটাৰ পৰমাণুৱে নিজৰ বহিৰতম কক্ষৰ পৰা ইলেক্ট্রন ত্যাগ কৰি বা বহিৰতম কক্ষত ইলেক্ট্রন গ্ৰহণ কৰি বা বহিৰতম কক্ষৰ ইলেক্ট্রন আন পৰমাণুৰ ইলেক্ট্ৰনৰ সৈতে ভাগ-বাটোৱাৰা কৰি নিকটতম সম্ভ্ৰান্ত গেছৰ সুস্থিৰ ইলেক্ট্রনীয় বিন্যাস লাভ কৰিবলৈ খোজে। ইয়াৰ বাবে মৌলটোৰ পৰমাণুৱে ত্যাগ কৰা, গ্ৰহণ কৰা বা ভাগ-বাটোৱাৰা কৰা ইলেক্ট্রনৰ সংখ্যাক মৌলটোৰ যোজ্যতা বোলে। উদাহৰণস্বৰূপে, মেগনেছিয়াম (12) ৰ ইলেক্ট্রনীয় বিন্যাস 2.8.2; সেয়েহে ই ইয়াৰ নিকটতম সম্ভ্ৰান্ত গেছৰ বিন্যাস লাভ কৰিবলৈ 2 টা ইলেক্ট্রন ত্যাগ কৰিব। সেয়েহে ইয়াৰ যোজ্যতা 2 । তেনেদৰে ছালফাৰ (16) ৰ ইলেক্ট্রনীয় বিন্যাস 2.8.6; সেয়েহে ই ইয়াৰ নিকটতম সম্ভ্ৰান্ত গেছৰ বিন্যাস লাভ কৰিবলৈ 2 টা ইলেক্ট্রন গ্ৰহণ কৰিব। এইবাবে ইয়াৰ যোজ্যতা 2।
প্রশ্ন 18. তলৰ তালিকাখনত পাৰমাণৱিক ভৰৰ বৰ্দ্ধিত ক্ৰমত তললৈ সজোৱা তিনিটা মৌলৰ কেইটামান গোট দিয়া হৈছে। কোনকেইটা গোটে ড’বেৰেইনাৰৰ ট্ৰায়াড গঠন কৰিব নির্ণয় কৰা। [HSLC 2022]
| গোট A | পাৰমাণৱিক ভৰ | গোট B | পাৰমাণৱিক ভৰ | গোট C | পাৰমাণৱিক ভৰ |
| N P S | 14.0 31.0 74.9 | Ca Sr Ba | 40.1 87.6 137.3 | Cl Br I | 35.5 79.9 126.9 |
উত্তৰঃ গোট B আৰু C য়ে৷ কাৰণ ড’বেৰেইনৰৰ ট্ৰায়াড একোটাত মাজৰ মৌলটোৰ পাৰমাণৱিক ভৰ বাকী দুটা মৌলৰ পাৰমাণৱিক ভৰৰ গড় মানৰ প্ৰায় সমান হয়।
গোট B ত Ca আৰু Ba ৰ গড় পাৰমাণৱিক ভৰ
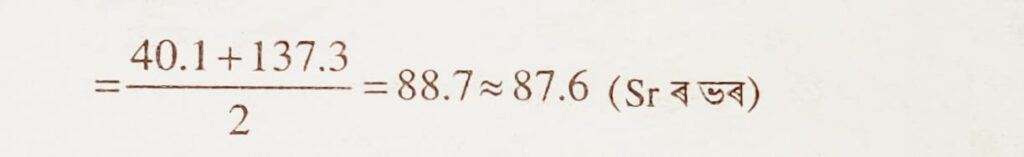
গোট C ত Cl আৰু I ৰ গড় পাৰমাণৱিক ভৰ
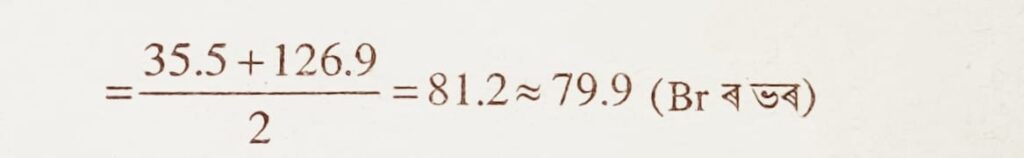
1 thought on “Class 10 Science Lesson 5 I মৌলৰ পৰ্যাবৃত্ত শ্রেণীবিভাজন”